2022年全國中藥材及飲片質(zhì)量分析概況
張萍 郭曉晗 金紅宇 姚令文 程顯隆 魏鋒 馬雙成
中國食品藥品檢定研究院,北京 102629
摘要
2022年初,,國務院辦公廳發(fā)布的《“十四五”中醫(yī)藥發(fā)展規(guī)劃》中提出加強中藥安全監(jiān)管,、提升中藥質(zhì)量評價能力、建立健全中藥質(zhì)量全鏈條安全監(jiān)管機制,、加強中藥飲片源頭管理等,,為推動中藥產(chǎn)業(yè)高質(zhì)量發(fā)展提出了明確的要求。2022年,,在國家藥品監(jiān)督管理局和各省藥品監(jiān)督管理部門的領導,、組織下,匯總?cè)珖兴幉募?/span>飲片的抽檢結(jié)果,,對全國31個省,、自治區(qū)、直轄市抽檢數(shù)據(jù)進行梳理并對總體質(zhì)量情況進行分析,,總體合格率為98%,。針對質(zhì)量和標準問題提出相關(guān)的監(jiān)管策略與建議,為提高中藥材及飲片標準,,提升監(jiān)管效力,、監(jiān)管水平提供大數(shù)據(jù)支持。
關(guān)鍵詞
中藥材 飲片 質(zhì)量 監(jiān)管
黨的二十大報告中明確提出要“強化食品藥品安全監(jiān)管”“促進中醫(yī)藥傳承創(chuàng)新發(fā)展”,,從國家戰(zhàn)略高度對中醫(yī)藥的發(fā)展進行了總體部署,。中藥產(chǎn)業(yè)作為中醫(yī)藥的重要組成部分,一直受到業(yè)界的普遍關(guān)注,,中藥材及飲片作為中藥產(chǎn)業(yè)的源頭,,其質(zhì)量好壞不僅關(guān)乎中藥產(chǎn)業(yè)的可持續(xù)發(fā)展,亦影響到公眾用藥的安全,、有效,。國家藥品監(jiān)督管理局每年度組織全國各地方藥品監(jiān)督管理部門進行監(jiān)督檢查和監(jiān)督抽檢工作,從源頭嚴抓產(chǎn)品質(zhì)量,,對中藥材及飲片進行了有力監(jiān)督和管理,,為中藥全產(chǎn)業(yè)鏈的健康、可持續(xù)發(fā)展提供重要保障,。
自2013年開展全國中藥材及飲片質(zhì)量抽檢工作以來,,中藥材及飲片的總體合格率由64%提升至98%,質(zhì)量呈持續(xù)向好的態(tài)勢,。雖然中藥材及飲片的質(zhì)量有了較大的提升,,但仍然存在摻偽摻雜[1-2],、染色增重[3]、不規(guī)范炮制[4-5],、重金屬及農(nóng)藥殘留超標[6]等質(zhì)量問題,。這些質(zhì)量問題已引起業(yè)界的高度關(guān)注,并從技術(shù)層面和監(jiān)管層面進行監(jiān)督指導,,鼓勵開展探索性研究,、推動建立補充檢驗方法、修訂完善質(zhì)量標準等,,這對提升產(chǎn)品質(zhì)量,,引領產(chǎn)業(yè)的健康、有序發(fā)展起到了較好的推動作用,。
2022年全國各地繼續(xù)開展省級抽檢工作,,雖然各地抽檢目的、抽樣環(huán)節(jié),、抽檢品種及覆蓋范圍等各有不同,,但總體抽檢數(shù)據(jù)和信息仍可以反映當前我國中藥材及飲片的質(zhì)量狀況。本文在全面匯總各省,、自治區(qū),、直轄市中藥材及飲片抽檢數(shù)據(jù)的基礎上,針對存在的問題進行了分析與探討,,并提出了相關(guān)監(jiān)管建議,形成2022年度《全國中藥材及飲片質(zhì)量分析報告》,,為持續(xù)提升中藥材及飲片質(zhì)量,、推動中藥產(chǎn)業(yè)源頭規(guī)范化管理提供依據(jù)。
一,、總體情況
2022年,,全國31個省,、自治區(qū),、直轄市(除港澳臺地區(qū))共抽檢中藥材及飲片46 888批,,合格45 749批,,從抽檢合格率看,各省,、自治區(qū),、直轄市的合格率均在90%以上,全國平均合格率為98%,,總體質(zhì)量狀況與2021年(抽檢51 194批,,合格49 807批,合格率97%)相比稍有提高,。進一步分析了近10年全國范圍的中藥材及飲片質(zhì)量抽檢數(shù)據(jù),結(jié)果表明,,2013—2022年中藥材及飲片質(zhì)量合格率逐年提高,,合格率從2013年的64%提升到2022年的近98%,體現(xiàn)了中藥材及飲片質(zhì)量逐年提升,、穩(wěn)步向好的發(fā)展態(tài)勢[7],,見圖1、圖2,。
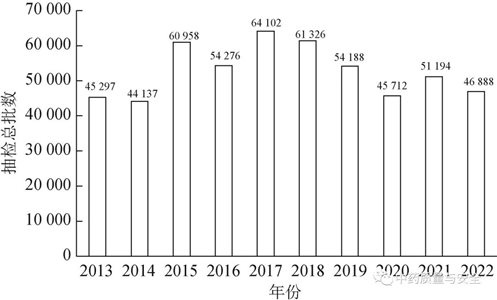
圖1 2013—2022年全國中藥材及飲片抽檢總批數(shù)
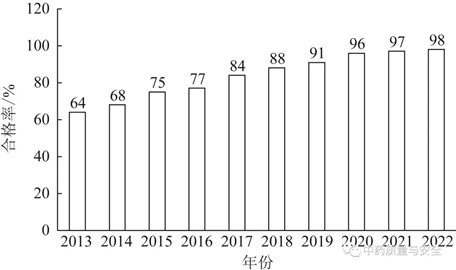
圖2 2013—2022年全國中藥材及飲片抽檢合格率
二,、主要問題及分析
(一)品種混用與摻偽問題
隨著中藥產(chǎn)業(yè)持續(xù)發(fā)展與擴大,對中藥材及飲片的需求日益激增,,中藥材及飲片資源不足的問題顯現(xiàn),,雖然有大量栽培藥材上市,,但從品種數(shù)量和生產(chǎn)規(guī)模方面遠滿足不了市場需求。市場上依然會出現(xiàn)一些近緣物種或混偽品作為正品藥材及飲片銷售,、使用的情況,即品種混用問題,,如毛雞骨草冒充雞骨草,、大葉茜草冒充茜草、川木通冒充木通,、小通草冒充通草,、山蘭冒充山慈菇[8]、雞冠花子冒充青葙子,、留蘭香冒充薄荷等[9],。另外,中藥材加工切制成飲片后,,因外觀形態(tài)受到部分破壞,,極易出現(xiàn)摻偽問題(包括同源摻偽),為檢驗工作帶來一定難度,。例如,,菟絲子中摻入千穗谷子,小通草中摻入西南繡球的莖髓[10],,酸棗仁中摻入滇棗仁,、拐棗仁等[11],。
針對上述問題,應當在充分調(diào)研的基礎上,,采用多學科技術(shù)手段,,積極開展探索性研究,從生藥學到分子,、理化檢測方面建立能有效甄別正品與偽品的方法,,進行中藥真?zhèn)舞b別。
(二)種植/養(yǎng)殖不規(guī)范引起藥材品質(zhì)下降
在國務院辦公廳《關(guān)于印發(fā)中醫(yī)藥振興發(fā)展重大工程實施方案的通知》(國辦發(fā)〔2023〕3號)[12]中提出,,要廣泛開展中藥材生態(tài)種植,、野生撫育和仿野生栽培,提出了規(guī)范化種植中藥材的目標和任務,,中藥材種植產(chǎn)業(yè)方興未艾,。目前,人工種植栽培的中藥材有近300種,,種植/養(yǎng)殖藥材品種占中藥資源總數(shù)的20%,,栽培種植藥材一定程度上緩解了中藥資源緊缺的問題。
在抽檢工作中也發(fā)現(xiàn)種植栽培藥材的一些質(zhì)量問題:首先,,由于栽培地土質(zhì)肥沃,,水分、養(yǎng)分充足導致人工種植的藥材通體較為飽滿,,質(zhì)地堅實,,外觀性狀、表面及斷面顏色,、質(zhì)地等與野生品的差異較大,。例如,苦參野生品飲片切面呈纖維性,,具放射狀紋理和裂隙,,而栽培苦參飲片切面纖維性差,未見裂隙,,性狀方面差異較大,。丹參、甘草樣品亦如此,。其次,,栽培藥材由于人為因素導致在較短時間內(nèi)快速生長,化學成分累積不夠,,提前采收或生長年限較短易出現(xiàn)浸出物或含量測定不合格的現(xiàn)象,。例如,丹參栽培藥材中丹參酮類含量不合格[13],,南五味子果實搶青采收會出現(xiàn)五味子酯甲含量不合格等,。再次,,種植栽培缺乏規(guī)范的生產(chǎn)質(zhì)量控制標準,種植過程中使用禁用農(nóng)藥,、化肥,,導致藥材中外源性重金屬或農(nóng)藥殘留超標[14],無法保證藥材質(zhì)量,。例如,,菊花樣品中檢出甲拌磷[15],金銀花中檢出氟啶蟲胺腈,、氟啶蟲酰胺和溴氰菊酯等[16],,人參中檢出六氯苯、五氯硝基苯,、六六六等[17]。此外,,尚缺乏常用中藥有害物質(zhì)殘留檢測數(shù)據(jù)庫,,也沒有全面地對可能的污染來源進行深入分析和監(jiān)測。忽視藥材的道地性或異地引種栽培的現(xiàn)象較為普遍,,這導致樣品質(zhì)量的差異性,,如不同產(chǎn)地甘草藥材中甘草苷和甘草酸的含量,道地產(chǎn)區(qū)內(nèi)蒙古的甘草中甘草苷和甘草酸的含量顯著高于非道地產(chǎn)區(qū)甘草中兩者 的含量[18],;厚樸道地產(chǎn)區(qū)(四川東部)與非道地產(chǎn)區(qū)的樣品存在較大的差異,,阿洛糖苯乙醇四糖二糖苷、阿洛糖苯乙醇四糖三糖苷及阿洛糖苯乙醇四糖四糖苷可作為厚樸的道地性判別指標[19],。推動道地產(chǎn)區(qū)中藥材的合理,、規(guī)范種植,探討道地藥材的“道地性”品質(zhì)特征,,從“辨狀論質(zhì)”,、基因等方面對道地藥材的成因進行綜合分析。
(三)不規(guī)范炮制影響飲片質(zhì)量
中藥炮制技術(shù)是中醫(yī)藥理論體系的重要組成部分,,中藥飲片通過炮制達到增強療效,、降低不良反應、緩和藥性,、引藥歸經(jīng)或改變作用趨向,、易于配方和調(diào)劑等目的,供臨床使用或中成藥制劑生產(chǎn)投料,。在2022年全國抽檢工作中,,依然發(fā)現(xiàn)不規(guī)范的炮制加工引起的飲片質(zhì)量問題。例如,,標示醋延胡索飲片的樣品,,表面和切面均顯示黃色,,不具醋香氣;標示炒紫蘇子的樣品,,未見表面有裂口,,不具焦香氣;標示蜜款冬花的樣品中款冬酮含量測定及雜質(zhì)項均不合格,;標示黃精飲片的樣品,,切面未呈現(xiàn)半透明角質(zhì)樣;標示鹽菟絲子的樣品,,未見表面有裂開,,僅口嘗有咸味等。
另外,,中藥飲片凈度不夠也是引起質(zhì)量不合格的因素之一,。中藥材來源于自然界植物、動物或礦物,,在采收,、加工、流通運輸?shù)拳h(huán)節(jié)難免混入泥沙及非藥用部位等雜質(zhì),,在藥材切制,、炮制前,須進行挑揀,、刮削,、篩選、去芯等工作,,以除去泥沙,、藥屑或非藥用部位雜質(zhì)。除雜不凈導致飲片樣品中雜質(zhì)超標的問題,,如桑葉中未去葉柄,、款冬花中未去花梗、柴胡飲片中未去地上莖部分,、動物藥內(nèi)臟未去除泥沙等,,這都會影響飲片的質(zhì)量。
對需要加輔料炮制的飲片,,輔料標準不統(tǒng)一也會影響其質(zhì)量,。炮制輔料主要包括液體輔料,如醋,、鹽,、酒、蜂蜜、姜汁等,,固體輔料,,如麥麩、米,、沙,、土、滑石,、明礬等,。輔料標準多參考食品、調(diào)味品,、飲品或藥品的標準,,沒有統(tǒng)一的制備工藝要求和控制標準,這對飲片的質(zhì)量會產(chǎn)生一定的影響[20-22],。另外,,發(fā)酵法屬于炮制技術(shù)中較難的復制法,發(fā)酵技術(shù)是影響各種曲類中藥及膽南星,、淡豆豉等需發(fā)酵中藥質(zhì)量的主要因素,,發(fā)酵原料不一致、工藝參數(shù)不一致,、環(huán)境有差異,尤其是發(fā)酵菌群的差異,,導致該類中藥的質(zhì)量較難控制,,并存在較大的差異性[23-24]。對于該類中藥,,應充分運用現(xiàn)代生物技術(shù)和相關(guān)設備,,優(yōu)化發(fā)酵炮制的處方原料,參與發(fā)酵的菌種類型,、數(shù)量,、比例,溫度,,濕度,,時間等參數(shù),實現(xiàn)發(fā)酵過程的自動化,、機械化和標準化,,實現(xiàn)發(fā)酵炮制過程可控,穩(wěn)定發(fā)酵品質(zhì)量,。還有諸如飲片切制不規(guī)范,、加熱干燥不規(guī)范等引起的質(zhì)量問題也不容忽視。
(四)儲存養(yǎng)護不當易產(chǎn)生發(fā)霉、蟲蛀等問題
中藥材及飲片在采收加工炮制后一般需要入庫進行儲存與養(yǎng)護,,按照其本身的性質(zhì)特點應進行分類儲存,。對易生蟲的品種,如山藥,、天花粉,、白芷、薏苡仁等宜集中存放,,便于殺蟲養(yǎng)護,;對易泛油及霉變的品種,如麥冬,、黃精,、柏子仁、黨參等宜陰涼,、干燥通風儲存,;對含揮發(fā)性物質(zhì)的品種,如丁香,、薄荷,、桂皮宜避光或密封儲存;對毒麻品種,,如馬錢子,、罌粟殼、甘遂,、狼毒等宜單獨分庫儲存,。合理控制儲存條件是保證中藥材及飲片質(zhì)量的重要環(huán)節(jié)之一[25],。2022年全國抽檢中發(fā)現(xiàn)飲片的質(zhì)量問題中,由蟲蛀和霉變引起的質(zhì)量不合格占比越來越多,,如槲寄生、板藍根,、白術(shù),、山楂,、紅花、粉葛、獨活等因蟲蛀而不合格,;瓜蔞,、巫山淫羊藿,、西洋參、豆蔻,、香櫞等因霉變而不合格,;薏苡仁,、檳榔、胖大海,、土茯苓、延胡索、柏子仁,、九香蟲等因黃曲霉毒素限度超標而不合格。含揮發(fā)性成分的品種放置后,易致?lián)]發(fā)油含量不合格,,如檀香,、蒼術(shù),、艾葉等。
除了適宜的儲存,對于中藥材及飲片而言,還需要更加精心的后期養(yǎng)護,,達到防蟲,、防潮,、防霉變的目的。目前,多采用硫黃熏蒸技術(shù)用于保存中藥材及飲片[26],但過度的硫黃熏蒸會使中藥材及飲片內(nèi)在成分發(fā)生變化,降低中藥材及飲片的質(zhì)量,,如硫熏桔梗使其桔梗皂苷D含量明顯降低[27],;百合經(jīng)硫熏后苯丙烯酸類和甾體皂苷類成分含量降低,,而產(chǎn)生新的系列含硫產(chǎn)物[28],;粉葛硫熏后無機元素Cr,、Mo、Cd,、Pb含量明顯增加,,而4?-O-甲基葛根素、黃豆黃苷和大豆苷含量降低明顯[29],。2022年檢出百合,、粉葛、山藥,、甘草,、黨參、白術(shù)等樣品中二氧化硫殘留超標,,過度硫熏不但影響中藥材及飲片的質(zhì)量,,還間接危害使用者的健康,應引起監(jiān)管部門的高度重視,,同時尋找安全,、有效的硫熏替代技術(shù)勢在必行。
(五)染色,、增重問題依然存在
中藥材及飲片染色問題由來已久,,一直是困擾產(chǎn)業(yè)健康發(fā)展的阻力之一,,究其染色原因有三:偽品染色充當正品用、次品染色充當優(yōu)質(zhì)品用,、藥渣染色再銷售使用,。為有效打擊違法染色造假行為,檢驗檢測機構(gòu)紛紛開展染色造假專項研究工作,,并及時發(fā)布補充檢驗方法[30],。目前,已頒布中藥材及飲片染色的補充檢驗方法20余種,,相關(guān)中成藥染色的補充檢驗方法近30種,,涉及的常用染色色素品種近20種,有效打擊了不法行為[31],。2022年檢出染色的品種較往年有所減少,,但增重的品種仍然存在,如通草中加明礬,、硫酸鎂,,全蝎加入食鹽,水蛭加入滑石粉等,,質(zhì)量問題不容忽視,。
(六)進口中藥材質(zhì)量參差不齊
進口中藥材作為我國中藥資源的來源之一,一直占有重要的地位,。據(jù)不完全統(tǒng)計,,我國現(xiàn)有進口中藥材品種約110種,約占中藥材品種的10%[32],,近90%進口品種來源于亞洲國家,。除了常規(guī)的進口中藥材品種,少數(shù)民族使用的一些特有藥材品種也多來自進口,。近10年來,,進口藥材品種和數(shù)量增長勢頭非常強勁,進口數(shù)量從4.7萬t增加到近20萬t[33],。對于進口藥材,,有的品種基礎研究薄弱,基原不清,、加工方法不明,;有的藥材在境外生產(chǎn)過程無法管控,質(zhì)量溯源難度大,,隨之出現(xiàn)了一些質(zhì)量問題,,如血竭有摻偽情況;乳香、沒藥為多來源品種,,揮發(fā)性成分含量差異較大,,并有摻偽情況,使得雜質(zhì)含量高,;猴棗基原不明確,;進口檳榔多有霉變發(fā)生;進口甘草中甘草苷含量不合格等,。另外,一些在國外種植的藥材其質(zhì)量問題也是不可忽視的,。建議對有問題的進口藥材品種進行基原調(diào)研,,加強進口藥材生產(chǎn)過程的有效管控,提升進口藥材的質(zhì)量標準,,把好質(zhì)量關(guān),,進而推動我國中藥產(chǎn)業(yè)的健康、可持續(xù)發(fā)展,。
針對上述問題,,對2022年全國中藥材及飲片檢驗情況進行了數(shù)據(jù)分析,匯總抽樣批次較多且不合格率較高的品種,,見表1,。

三、監(jiān)管措施及建議
(一)強化中藥材種植/養(yǎng)殖管理,,建立藥材種子及種苗的規(guī)范管理體系
繁育優(yōu)質(zhì)中藥材種子種苗是中藥材生產(chǎn)的關(guān)鍵,,也是保證中藥材質(zhì)量穩(wěn)定的重要因素。目前,,我國中藥材種子種苗存在假種劣種混雜,、育種的投入和產(chǎn)出倒掛、種子的品質(zhì)評價缺乏客觀標準,、監(jiān)管力度不足等問題,,制約了中藥材前端種植產(chǎn)業(yè)的發(fā)展。我國人工栽培種植的中藥材近200種,,培育出優(yōu)良品種并在生產(chǎn)上推廣應用的藥材品種不足20種,,中藥材種子種苗的繁育基本上處于自繁自用階段,中藥材繁育,、選育嚴重滯后,,極大限制了中藥材生產(chǎn)技術(shù)水平的提高。因此,,在推動中醫(yī)藥產(chǎn)業(yè)規(guī)范化,、標準化的大背景下,應建立中藥材種子種苗的規(guī)范管理體系,包括種質(zhì)資源標準,、優(yōu)良品種選育標準,、良種繁育生產(chǎn)標準、種子種苗檢測標準規(guī)范化,,從源頭對中藥材種植/養(yǎng)殖進行標準規(guī)范管理,,提升中藥產(chǎn)業(yè)國際競爭力。同時,,加強農(nóng)業(yè)部門和藥品監(jiān)督管理部門的協(xié)調(diào)運作,,明確管理職責,對種子種苗規(guī)范化進行科學論證,,制定種子種苗撫育發(fā)展規(guī)劃,,實現(xiàn)中藥材種子種苗的標準化,從源頭保證中藥材質(zhì)量,。
(二)重視并進一步規(guī)范藥材產(chǎn)地初加工管理
藥材采收后,,大部分需根據(jù)其性質(zhì)和銷售、運輸,、保管的要求在產(chǎn)地進行初步加工處理,,以防止變質(zhì)霉爛,也便于藥材的進一步加工炮制及貯存,、包裝等,,產(chǎn)地初加工是中藥材質(zhì)優(yōu)的重要環(huán)節(jié)和保證。新修訂的《中華人民共和國藥品管理法》[34]中僅規(guī)定中藥飲片必須按國家藥品標準進行炮制,,并沒有針對中藥的產(chǎn)地初加工過程進行規(guī)范,。在《中藥材生產(chǎn)質(zhì)量管理規(guī)范》(GAP)[35]中僅提到了產(chǎn)地初加工的框架構(gòu)建,缺少相關(guān)的加工標準和規(guī)范細則,。多年來產(chǎn)地初加工一直是監(jiān)管的薄弱環(huán)節(jié),,缺乏有效的監(jiān)管手段,存在產(chǎn)地初加工企業(yè)小而散,、加工設備簡陋,、加工方法有地域性差異等問題,導致“一藥多法”現(xiàn)象屢屢出現(xiàn),。另外,,在產(chǎn)地初加工階段,有的采用摻雜使假,、以劣充優(yōu)等非法手段,,嚴重影響中藥材的質(zhì)量。因此,,為保證中藥材的質(zhì)量,,應從法規(guī)層面上重視和加強中藥材產(chǎn)地初加工管理,,在充分了解中藥材的特殊性、立足產(chǎn)地道地性的基礎上,,優(yōu)化產(chǎn)地初加工模式,,以產(chǎn)地初加工技術(shù)為切入點,結(jié)合生產(chǎn)實際,,建立以產(chǎn)地初加工通用技術(shù),、加工設備要求及運輸儲存為主的科學的產(chǎn)地加工流程及技術(shù)標準,構(gòu)建基于中藥材道地屬性的產(chǎn)地初加工管理規(guī)范體系,。
(三)逐步推進中藥飲片批準文號及有效期(保質(zhì)期)管理
中藥飲片作為臨床用藥和中成藥投料原料,,長期以來備受關(guān)注。近年來發(fā)現(xiàn)的中藥飲片染色,、增重,、摻雜使假、非法加工,、違規(guī)經(jīng)營等問題,,加之炮制不按工藝進行,、加工生產(chǎn)車間未認證,,甚至從市場采購飲片分袋貼標等情況,一定程度暴露了中藥飲片生產(chǎn)門檻較低,、缺乏實施批準文號管理的弊端,。目前,僅有包括冰片,、阿膠等在內(nèi)的15種中藥飲片按批準文號管理,。2004年國家藥品監(jiān)督管理局會同國家中醫(yī)藥管理局聯(lián)合發(fā)布了《關(guān)于實施批準文號管理的中藥飲片品種目錄》征求意見稿(70種),但遲遲沒有落地,。隨著中藥產(chǎn)業(yè)的有序發(fā)展,,可對亟須加強管理的品種及科研基礎較好的品種分期分批、積極穩(wěn)妥地推進實施批準文號管理,,為藥品生產(chǎn)經(jīng)營企業(yè)提供品種目錄,、為基層執(zhí)法提供執(zhí)法依據(jù)。實施批準文號管理可進一步規(guī)范中藥飲片的生產(chǎn),、完善藥品監(jiān)督管理體系,、牢固樹立質(zhì)量意識、優(yōu)勝劣汰,、增強中藥競爭力,、保護公眾的用藥安全。
根據(jù)《藥品管理法實施條例》[36]及《藥品說明書和標簽管理規(guī)定》[37]的相關(guān)要求,,除對實行批準文號管理的中藥飲片需按標注的有效期進行管理外,,對未實行文號管理的中藥飲片目前尚沒有進行有效期管理。另外,現(xiàn)行版《藥品生產(chǎn)質(zhì)量管理規(guī)范(GMP)》中也未對中藥飲片規(guī)定有效期(保質(zhì)期)管理,,導致有的飲片在儲存時會因儲存時間及儲存條件等發(fā)生蟲蛀,、霉變的質(zhì)量問題。雖然有的品種在包裝袋上規(guī)定了有效期或保質(zhì)期,,這僅是企業(yè)行為,,缺少國家的相關(guān)法律、法規(guī)規(guī)定,。中藥飲片沒有有效期管理易導致監(jiān)管執(zhí)法難,、不能依法打擊銷售假劣藥行為、病患維權(quán)難,,難以保證用藥安全,。因此,對于易霉變易蟲蛀及含揮發(fā)性成分的中藥材及飲片應盡快制定中藥飲片有效期(保質(zhì)期)管理,,既保證醫(yī)療單位的質(zhì)量管理體系有序運行,,又保證中成藥生產(chǎn)企業(yè)的質(zhì)量管理,為中藥飲片的出口創(chuàng)匯提供有力保證,,同時為中藥與國際植物藥管理接軌提供保障,。
(四)亟須規(guī)范硫黃熏蒸中藥材及飲片加工技術(shù),積極推廣無硫加工方法
硫黃熏蒸中藥材是一種傳統(tǒng)的加工技術(shù),,硫黃經(jīng)加熱升華釋放出硫黃分子,,分布在中藥材及飲片表面,形成1層均勻的保護膜,,達到殺菌防霉,、防蟲蛀及漂白等作用,在中藥材及飲片的儲藏,、保管方面發(fā)揮一定的積極作用,。但硫黃加熱產(chǎn)生的二氧化硫也是一種強還原劑,能與中藥材及飲片中的某些成分發(fā)生化學反應,,使有效成分的含量下降,,甚至影響臨床療效。同時,,表面殘留的二氧化硫等對用藥健康構(gòu)成了安全隱患[38],。如何有效規(guī)范該項熏蒸技術(shù)成為中藥材及飲片安全生產(chǎn)的重大挑戰(zhàn)。
目前,,硫黃熏蒸技術(shù)缺少標準的操作規(guī)范,,加工車間廠房、熏蒸設備缺少統(tǒng)一標準,,熏蒸時間,、硫黃用量,、中藥材及飲片用量均沒有標準的技術(shù)要求,硫黃熏蒸仍處于散亂狀態(tài),,亟須建立中藥材熏蒸加工技術(shù)規(guī)范,,引導硫黃熏蒸傳統(tǒng)技術(shù)規(guī)范發(fā)展。另外,,隨著新型干燥技術(shù)的發(fā)展,,出現(xiàn)了越來越多的新型干燥設備,使得中藥材及飲片加工方法越來越多,,尋找替代硫黃熏蒸加工的呼聲逐漸高漲,。無硫加工是目前應用最廣的技術(shù)之一,該技術(shù)包括真空冷凍干燥加工,、噴霧干燥加工,、微波快速干燥、鈷60輻照加工等,,這些技術(shù)均具有良好的市場應用前景,。尋找操作簡單、有效成分流失少,、不影響藥效,、不產(chǎn)生不引入有害物質(zhì)等優(yōu)點的無硫中藥材及飲片加工方法,依然是生產(chǎn)加工中亟待解決的問題[39],。
(五)完善中藥材及飲片質(zhì)量溯源體系建設
中藥產(chǎn)業(yè)是全鏈條產(chǎn)業(yè),,涉及種子種苗,、種植/養(yǎng)殖,、采收加工、炮制,、儲存保管,、運輸流通、投料及臨方配制使用等多環(huán)節(jié),,每一個環(huán)節(jié)都與質(zhì)量相關(guān),,質(zhì)量貫穿于中藥產(chǎn)業(yè)的始終,推進中藥產(chǎn)業(yè)質(zhì)量追溯體系建設一直是行業(yè)關(guān)注的重點,。國家藥品監(jiān)督管理局多次強調(diào)要積極探索建立中藥材,、飲片及中成藥生產(chǎn)流通使用全過程追溯體系,依法加強中藥材質(zhì)量監(jiān)測,,組織中藥材及飲片抽檢并定期公布抽檢結(jié)果,,將中藥飲片質(zhì)量管理向前延伸到中藥材產(chǎn)地管理,推進和強化中藥材信息化追溯平臺建設,,實現(xiàn)中藥材種植,、采收,、加工、干燥,、包裝,、儲存及銷售等全過程可追溯,促進中藥材規(guī)范化發(fā)展,,加強中藥質(zhì)量源頭控制,,并定期開展GAP檢查等,從監(jiān)管層面為質(zhì)量溯源體系建設把關(guān)診脈,。
建議以問題為導向,,運用風險評估分析將問題消滅于萌芽狀態(tài),進一步推進風險評估制度的建設,。同時,,運用市場監(jiān)管這一杠桿,向上下游延伸,,督促中藥材種植戶,、飲片生產(chǎn)企業(yè)及中成藥企業(yè)落實質(zhì)量主體責任,推進中藥材及飲片,、中成藥的質(zhì)量持續(xù)穩(wěn)步提升,,守住中藥質(zhì)量與安全這一底線,為中醫(yī)臨床服務提供保障,。穩(wěn)步推進藥品信息化追溯體系建設,、制定藥品追溯相關(guān)技術(shù)標準、統(tǒng)一藥品追溯標準規(guī)范,、建立藥品基礎數(shù)據(jù)備案系統(tǒng),,推進中藥材及飲片生產(chǎn)經(jīng)營全過程溯源體系建設,實現(xiàn)中藥“來源可查,、去向可追,、責任可究”,體現(xiàn)“四個最嚴”要求,。
(六)齊抓共管,,全面推進GAP管理,,促進中藥高質(zhì)量發(fā)展
中藥材的全過程生產(chǎn)離不開規(guī)范的管理,,生產(chǎn)過程與質(zhì)量息息相關(guān),。新版GAP的發(fā)布實施,為中藥材的規(guī)范管理提出了更高更全面的要求,。在地方政府,各級監(jiān)管部門,,農(nóng)業(yè),、林業(yè)及中醫(yī)藥管理部門的監(jiān)督檢查、鼓勵扶持,、規(guī)劃指導下,充分調(diào)動中藥材生產(chǎn)企業(yè),、中藥生產(chǎn)企業(yè)的主觀能動性,變“要我”為“我要”,,增強質(zhì)量責任意識,,從種植/養(yǎng)殖源頭嚴把質(zhì)量關(guān)。對于中藥材生產(chǎn)企業(yè),鼓勵建設符合GAP要求的中藥材基地,按GAP生產(chǎn)的中藥材,,可以在產(chǎn)品標簽上標示“藥材符合GAP要求”,倡導優(yōu)質(zhì)優(yōu)先,優(yōu)質(zhì)優(yōu)價,發(fā)揮種植戶的積極性和主觀性,依靠各級主管部門的幫扶,、指導,,帶動GAP基地建設良性循環(huán)發(fā)展,,以點帶面,以面帶片,,推而廣之。對于中藥生產(chǎn)企業(yè),,建議使用符合GAP的中藥材及飲片做原料藥,,并鼓勵自建或與種植戶共建符合GAP要求的中藥材生產(chǎn)企業(yè)及生產(chǎn)基地,使中藥生產(chǎn)企業(yè)和中藥材生產(chǎn)企業(yè)成為真正的利益共同體,,將藥品質(zhì)量管理體系向前延伸到中藥材產(chǎn)地,。各級相關(guān)管理部門在進行督導檢查的同時,多給予技術(shù)支持,、政策引導,。藥品監(jiān)督管理部門做好延伸檢查。延伸指導工作,,與各級相關(guān)管理部門通力協(xié)作,,共同推進中藥材規(guī)范化、標準化,、集約化發(fā)展,,實現(xiàn)中藥上下游產(chǎn)業(yè)的融合與貫通,為優(yōu)質(zhì)優(yōu)價提供可能,,推動中藥高質(zhì)量發(fā)展,。
參考文獻
1.張萍,郭曉晗,,金紅宇,,等.2021年全國中藥材及飲片質(zhì)量分析[J].中國現(xiàn)代中藥,2022,,24(6):939-946.
2.張萍,,郭曉晗,,荊文光,等.2020年全國中藥材及中藥飲片質(zhì)量情況分析[J].中國現(xiàn)代中藥,,2021,,23(10):1671-1678.
3.林春燕.蒲黃,、草蒲黃藥材及其飲片的質(zhì)量分析和標準研究[D].昆明:云南中醫(yī)學院,,2018.
4.郭曉晗,張萍,,荊文光,,等.從2020年國家藥品抽檢專項有關(guān)問題談中藥材及中藥飲片監(jiān)管[J].中國現(xiàn)代中藥,2021,,23(10):1679-1685.
5.荊文光,,程顯隆,張萍,,等.2021年國家藥品抽檢飲片專項品種有關(guān)問題及建議[J].中國現(xiàn)代中藥,,2023,25(5):977-983.
6.孔繁越.中藥材重金屬限量標準和農(nóng)殘限量標準研究及標準制定相關(guān)建議[D].北京:北京中醫(yī)藥大學,,2017.
7.張萍,,李寧新,李明華,,等.2019年全國中藥材及飲片質(zhì)量分析報告[J].中國現(xiàn)代中藥,,2020,22(5):663-671.
8.郝壯壯,,曹宇欣,,劉朦朦,等.基于HPLC指紋圖譜及多指標成分測定結(jié)合化學計量學的不同商品規(guī)格山慈菇質(zhì)量差異分析[J].中草藥,,2023,,54(6):1935-1945.
9.崔宇宏,高天愛,,安志強.薄荷及其偽品留蘭香的鑒別[J].光明中醫(yī),,2011,26(8):1712-1714.
10.張純,,薛磊冰,,金佩芬,等.市售小通草質(zhì)量現(xiàn)狀調(diào)查及評價[J].中國現(xiàn)代應用藥學,,2017,,34(6):854-857.
11.張霞,郭盛,,王天舒,,等.基于圖像顏色及紋理特征的真偽酸棗仁鑒別方法研究[J].中藥材,,2022,45(10):2346-2351.
12.國務院辦公廳.關(guān)于印發(fā)中醫(yī)藥振興發(fā)展重大工程實施方案的通知(國辦發(fā)〔2023〕3號)[EB/OL].(2023-02-28)[2023-04-02].https://www.gov.cn/gongbao/content/2023/content_5747262.htm.
13.周仔莉,,李鵬,,陳雪琴,等.基于多指標成分分析及化學計量學的丹參道地性與飲片等級評價研究[J].現(xiàn)代中藥研究與實踐,,2023,,37(1):56-63.
14.劉芫汐,辜冬琳,,茍琰,,等.中藥材種植中農(nóng)藥使用情況及殘留現(xiàn)狀分析[J].中國藥事,2022,,36(5):503-510.
15.王瑩,,劉芫汐,劉麗娜,,等.中藥中外源性有害殘留物標準現(xiàn)狀與監(jiān)管建議[J].中國現(xiàn)代中藥,,2023,25(5):943-950.
16.王玉潔.溴氰菊酯,、氟啶蟲胺腈,、氟啶蟲酰胺三種農(nóng)藥在金銀花上的殘留規(guī)律及膳食風險研究[D].北京:北京協(xié)和醫(yī)學院,2017.
17.譚樂俊,,林林,,梅桂雪,等.人參鮮品中農(nóng)藥殘留評價研究[J].中南藥學,,2023,,21(2):508-514.
18.ZHANG X M,GUO X H,,ZHAO P,,et al.Chemometric analysis of active compounds and antioxidant and α-glucosidase inhibitory activities for the quality evaluation of licorice from different origins[J].Biomed Chromatogr,2021,,35(12):e5215.
19.XUE Z Z,,ZHANG X B,PENG H S,,et al.Exploration of habitat-related chemomarkers for Magnoliae officinaliscortex applying both global and water-soluble components-based metabolomics method[J].Phytomedicine,,2022,98:153957.
20.劉爽,,張振凌,,李軍,等.基于主成分分析法評價不同種類輔料對酒白芍飲片的影響[J].中藥材,,2019,,42(1):78-82.
21.周友紅,,吳國學,呼海濤.不同種類酒炮炙對牛膝飲片浸出物的影響[J].中國中醫(yī)藥現(xiàn)代遠程教育,,2010,,8(11):251-252.
22.程立平,顧雪竹,,毛淑杰.不同類型醋對小鼠的急性毒性及炮制延胡索鎮(zhèn)痛作用比較[J].中國實驗方劑學雜志,,2010,16(2):71-72.
23.王玉霞,,毛鑫,,王熠,,等.六神曲炮制歷史沿革及現(xiàn)代研究[J].時珍國醫(yī)國藥,,2017,28(5):1182-1184.
24.施宇,,劉曉峰,,單麗倩,等.膽南星發(fā)酵菌種的分離鑒定與復合菌種發(fā)酵初探[J].中國實驗方劑學雜志,,2022,,28(17):150-156.
25.邱尤娜,黃凱.中藥材與中藥飲片在庫房管理中存在的問題與規(guī)范化質(zhì)量控制[J].中醫(yī)藥管理雜志,,2023,,31(1):116-118.
26.胡佳偉,沈明勤,,李松林.硫磺熏蒸對中藥材品質(zhì)影響及其替代技術(shù)研究進展[J].國際藥學研究雜志,,2016,43(6):1054-1058.
27.戴光霞,,葛秀允.硫磺熏蒸對桔梗化學成分和藥效影響的實驗研究[J].中國藥業(yè),,2023,32(7):60-63.
28.張蓉,,楊亞玲,,鄧愛平,等.硫熏對百合藥材質(zhì)量和安全的影響[J].中國中藥雜志,,2023,,48(3):660-671.
29.陳鳳,梁秋云,,張曉娟,,等.硫熏對粉葛中無機元素與異黃酮類成分含量的影響[J].中藥材,2022,,45(9):2097-2102.
30.陳霞,,張永文,,周剛.中藥補充檢驗方法和檢驗項目相關(guān)問題探討[J].中國新藥雜志,2021,,30(21):1949-1955.
31.鐘名誠,,饒偉文,劉劍云.中藥染色摻假檢測方法的研究進展[J].海峽藥學,,2018,,30(5):32-35.
32.賈敏如,李心怡,,盧曉琳,,等.近代中國各民族使用進口傳統(tǒng)藥物(藥材)的品種分析及建議[J].華西藥學雜志,2019,,34(4):413-420.
33.于志斌,,李得運,劉麗娜,,等.2010—2019年藥材進口貿(mào)易情況及法規(guī)標準體系分析[J].中國現(xiàn)代中藥,,2022,24(1):147-152.
34.中華人民共和國全國人民代表大會常務委員會.中華人民共和國藥品管理法[EB/OL].(2019-08-26)[2023-05-02].https://www.gov.cn/xinwen/2019-08/26/content_5424780.htm.
35.國家藥品監(jiān)督管理局,,農(nóng)業(yè)農(nóng)村部,,國家林業(yè)和草原局,國家中醫(yī)藥管理局.關(guān)于發(fā)布《中藥材生產(chǎn)質(zhì)量管理規(guī)范》的公告(2022年第22號)[EB/OL].(2022-03-17)[2022-05-17].https://www.nmpa.gov.cn/xxgk/fgwj/xzhgfxwj/20220317110344133.html.
36.國家藥品監(jiān)督管理局.中華人民共和國藥品管理法實施條例)[EB/OL].(2019-03-02)[2022-05-17].https://www.nmpa.gov.cn/xxgk/fgwj/flxzhfg/20230328161255 114.html.
37.國家市場監(jiān)督管理總局.藥品說明書和標簽管理規(guī)定(局令〔第24號〕)[EB/OL].(2016-03-15)[2023-05-02].https://www.samr.gov.cn/zw/zfxxgk/fdzdgknr/bgt/art/2023/art_b1a64fa4b9314ecabadf3c6662b70c48.html.
38.陸兔林,,寧子琬,,單鑫,等.硫磺熏蒸對中藥材化學成分和藥理作用影響的研究進展[J].中國中藥雜志,,2014,,39(15):2796-2800.
39.吳秋麗,楊曉賓,,俞信光,,等.中藥材原產(chǎn)地無硫加工技術(shù)研究進展[J].科技創(chuàng)新導報,2017,,14(32):79-80.